直接压片(DC)是制药工业中理想的片剂生产工艺。与湿法制粒(WG)相比,它带来了许多好处。
直压可以缩短生产过程,并通过消除湿法制粒和干燥步骤减少能源消耗。因此,它可以显著降低生产的总成本。另一个优点是在处理对热或潮湿敏感的活性药物成分(API)时具有更高的稳定性¹。
甲芬那酸(MA)在BCS中被列为II类药物,具有较差的水溶性和高渗透率²。它是一种非甾体抗炎药,用于治疗与关节炎、肌肉紊乱和头痛相关的疼痛或肿胀症状³。对市售产品的评估表明,含有500mg甲芬那酸片剂大多通过湿法制粒方法生产的。
在本研究中,开发了采用直压工艺生产的含500mg甲芬那酸速释(IR)薄膜包衣片剂,配方如表1示。
甲芬那酸速释片研究
甲芬那酸、无水磷酸氢钙DI-CAFOS®A150(F20170000063已激活-布登海姆)、磷酸钙TRI-CAFOS®200-7、微晶纤维素MCC(推荐:F20180000805已激活-东辰制药)、交联羧甲纤维素钠、羟丙纤维素、硬脂酸镁、薄膜包衣剂。
表1:甲芬那酸速释片配方
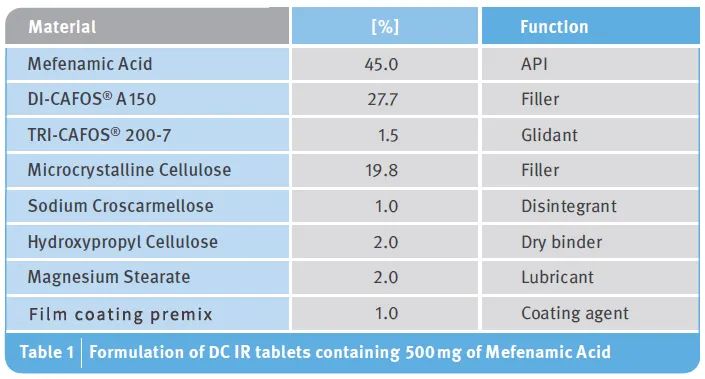
方法
1、将表1所示配方的所有成分除硬脂酸镁外,过筛(1.0mm),并在T10B型搅拌机中以32转/分的速度混合10分钟;将硬脂酸镁过筛(0.5mm),与之前混合后的物料以相同速度混合3分钟,批次为1kg。
2、用19x8.9mm刻痕椭圆形冲头的Fette 102i旋转压片机进行压片,转速分别为30和60rpm,压片时的压力为27kN,预压力为2.8kN。
3、调整片芯重量为1100mg,以达到每片含量500mg甲芬那酸的目标,包衣过程在Solidlab 1包衣机中进行,增重1%,用Smart-Test 50分析片剂重量、硬度、厚度、长度和宽度。
4、根据USP<1216>方法进行脆碎度分析。按照USP<701>,使用DisiTest 50仪器在水中测量崩解时限。在USP仪器中加入900mL tris缓冲溶液进行60分钟溶出试验,使用Pharmatest t70分光光度计在334nm处以1mm流速通过比色皿测量紫外吸收。
结果与讨论
表1所示的配方是为了实现直压工艺而设计的。本研究的甲芬那酸具有非常差的流动性、可压性。其休止角为84°,堆密度为0.3g/mL,颗粒非常细,D50小于13μm,这使得直压工艺具有挑战性。与市售产品性能进行比较,见表2。
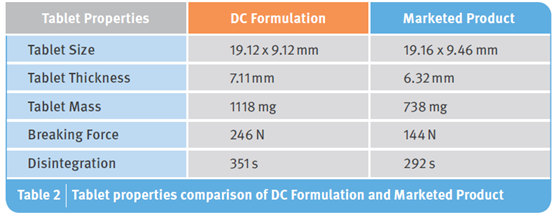
两种制剂的片剂尺寸非常相似,市售产品的宽度和长度略大于直压制剂。湿法制粒的优点之一是增加了粉末的堆密度,这使得片剂更薄更轻,就像市售片剂一样。
然而,羟丙纤维素作为干粘合剂,结合无水磷酸氢钙和微晶纤维素的脆性和塑性形变,提高了直压配方中的片剂硬度,高于市售产品。两种制剂的崩解时限相当,均在ICH (Q4B附录5)要求的速释膜包衣片验收标准60分钟内。
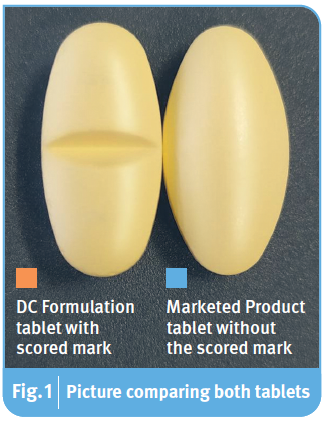
图1.两种制剂对比图
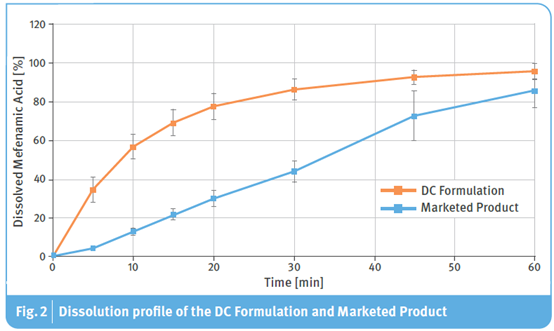
图2.直压制剂与市售产品溶出度
两种制剂的溶出曲线如图2所示,这验证了本研究中两种工艺间的显著差异。所开发的直压片剂甲芬那酸在20分钟内的溶出度约80%,而市售产品在50分钟后才达到相同的溶出度。此外,有部分市售产品不符合USP验收标准,根据该标准,原料药在45分钟后溶出度不少于75%。
本研究成功开发出含500mg甲芬那酸速释片制剂。该制剂具有机械强度好、溶出速度快的特点,在这些方面优于湿法制粒生产的市售产品。

Copyright © 2025 深圳市优普惠药品股份有限公司 版权所有 互联网药品信息服务资格证书:(粤)-非经营性-2023-0304