乙酰水杨酸
非甾体抗炎药(NSAID)乙酰水杨酸(ASA)是世界上使用最广泛的药物之一,具有抗炎、解热和镇痛作用。根据其适应症,使用的剂量为100-1000 mg ASA。[1] 与咖啡因组合使用可增强ASA的药理作用。[2] ASA通过水解(主要是与水接触)分解,可产生水杨酸和乙酸。[3] 因此API与赋形剂结合的稳定性,特别是考虑其水分敏感性,对于药物制剂至关重要。
据报道,ASA在55℃和75% r.H.条件下不会降解,而辅料微晶纤维素的加入会在相同条件下引起降解问题。[4] 这与微晶纤维素的弱吸附水有关。[5] 与另一种常见的辅料磷酸氢钙二水合物组合使用时,则会出现因失去结晶水而导致的ASA稳定性问题。[6]
本研究的目的是研究ASA在含有以下稀释剂的制剂中的稳定性,这三种稀释剂分别是:无水磷酸氢钙、磷酸氢钙二水合物和微晶纤维素。此外,,还研究了辅料粉末表面积增大对ASA稳定性的影响。另外,还考察了片剂在20kN和30 kN压片力下的性能变化。试验在12周内设置了两种不同的放置条件:①22.5℃和40% r.H.或②40℃和70% r.H.。
物料及方法
配方:
表1.乙酰水杨酸片配方表(片重600mg)
乙酰水杨酸颗粒 | 41.67% |
咖啡因颗粒 | 8.33% |
交联羧甲基纤维素钠 | 2% |
硬脂酸镁 | 0.5% |
稀释剂 | 47.5% |
设备:旋转压片机 模具:Euro-B型10mm 压力:20-30kN | |
其中三种稀释剂分别为:无水磷酸氢钙(布登海姆A60),磷酸氢钙二水合物(布登海姆D160),微晶纤维素(102)。

图1. A60电镜图
方法:
压片:将含有4ASA、咖啡因、稀释剂、交联羧甲基纤维素钠和硬脂酸镁的片剂混合物,在20-30kN压力下,压制成600 mg重量的片剂。
放置:在以下两种条件(①22.5℃,40% r.H.或②40℃和70% r.H.)下将所制片剂放置12周。除制得片剂外,还有粉末混合物,以便对ASA的稳定性进行评估。粉末混合物由1:1的API和稀释剂组成。粉末的放置条件与片剂的放置条件相同。作为参考,还放置了API-ASA。此外,粉末以研磨过(G)和未研磨(NG)两种形式放置,以评估增大表面积是否会对结果造成影响。研磨是用研钵和研杵以手工完成的。通过HPLC法对ASA降解产物水杨酸进行了测量。
结果与讨论
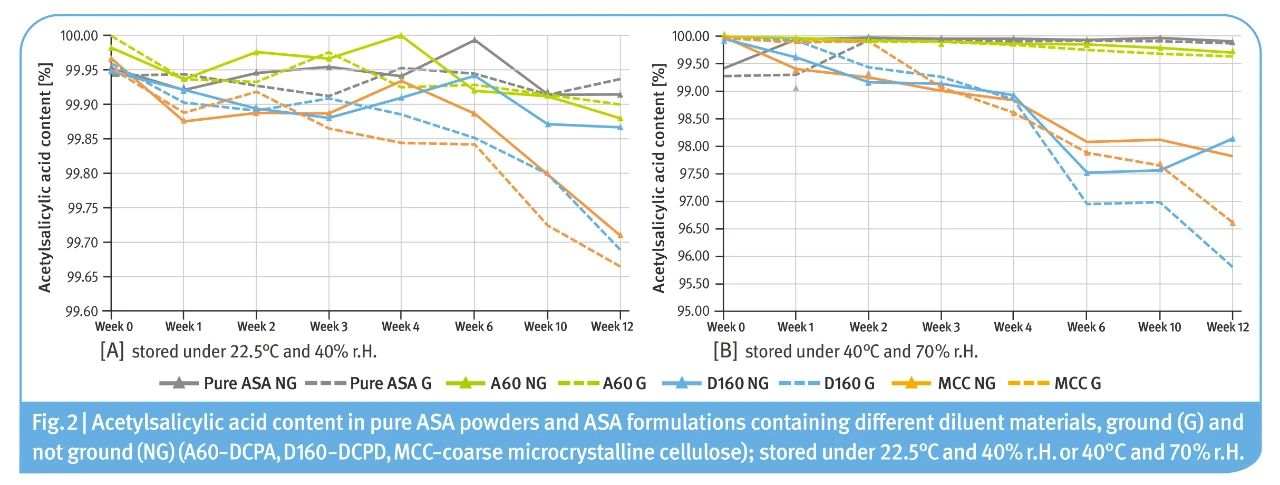
图2. 纯ASA粉末和ASA 处方中乙酰水杨酸含量(包含研磨(G)和未研磨(NG)稀释剂)(A60,D160,MCC)
在放置于22.5℃和40% r.H.条件下的ASA-稀释剂混合物中(图2),观察到:
>>>含MCC和DCPD粉末(均为研磨粉末)的ASA含量略有下降,分别下降到99.67%和99.69%。对于含DCPA的粉末和纯ASA物料,几乎没有观察到降解效果。未发现研磨和未研磨物料存在相关差异。
>>>在较高的湿度和温度水平下(40℃和70% r.H.),可以观察到ASA的降解加剧。MCC粉末(未研磨)的ASA含量降至96.61%,DCPD粉末(研磨)的ASA含量降至95.81%。DCPA混合物中的ASA和纯ASA几乎未受影响:分别为99.64%和99.91%。没有观察到表面积增大和水解度更高之间存在相关性。
>>>对放置片剂(未显示)中乙酰水杨酸降解的分析显示了类似的结果。在含MCC和DCPD的片剂中,ASA的降解度最高,而含DCPA片剂的ASA水解度最低。没有观察到咖啡因对ASA的降解存在影响。
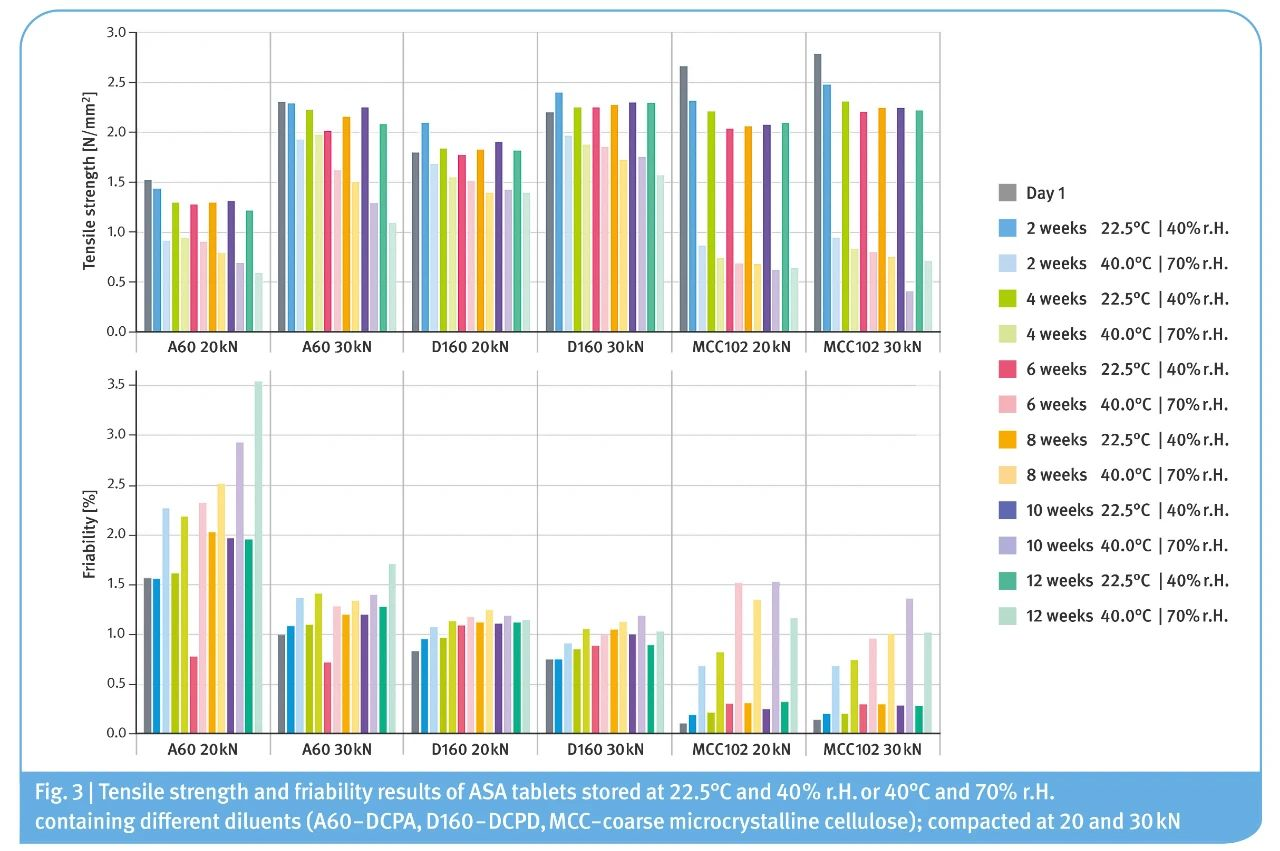
图3.在22.5°C和40% r.H.或40°C和70% r.H.下放置的包含不同稀释剂的ASA片拉伸强度和脆碎度结果(A60, D160,MCC); 20和30kN压片
对放置片剂的研究(图3)显示:
>>>对于所有使用的辅料,在放置时间内的两种放置条件下,片剂的拉伸强度都普遍下降。40℃和70% r.H.条件下拉伸强度的下降程度大于22.5℃和40% r.H.条件下拉伸强度的下降程度。
>>>对于含有MCC的片剂,拉伸强度下降程度较大,降低到初始值的67%,这种影响是显著的。此外,由于MCC片剂在40℃和70% r.H.条件下膨胀,其厚度增加了12%。
>>>观察到DCPA处方的脆碎度最高。但是,还可以观察到MCC片剂在40℃和70% r.H.条件下的脆碎度增加。在两种放置条件下,含DCPD的片剂的脆碎度均没有明显变化。
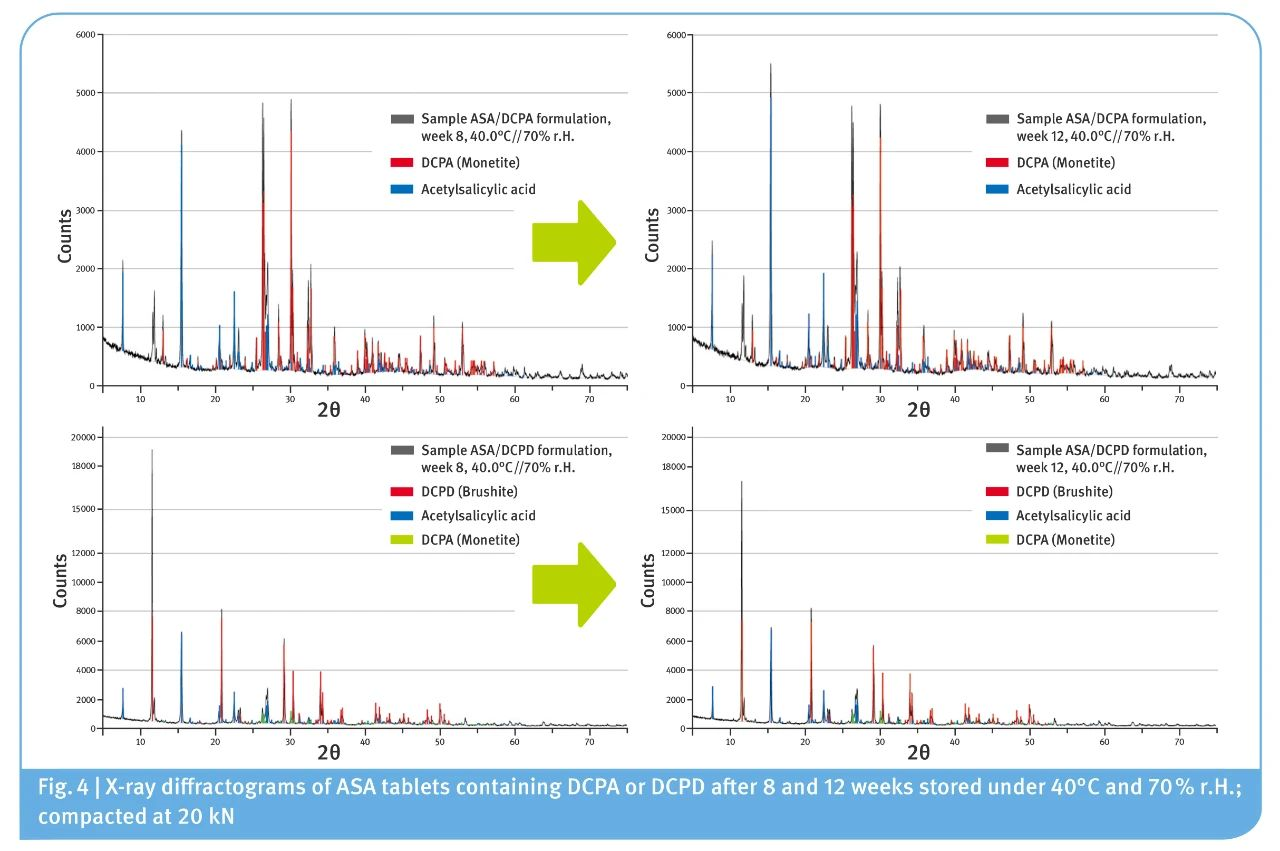
图4. 40°C和70% r.H.下放置8周和12周的包含DCPA或DCPD的ASA片的X-射线衍射图; 20 kN压片
图4结果显示:
>>>就晶体结构而言,DCPA和DCPD片剂在不同放置条件和放置时间之间的差异是显而易见的。对放置8周的DCPD片剂的研究显示,两种放置条件下DCPA的量均为6%(±1%)
>>>在第0周、第12周的片剂和DCPD物料中也发现了相同量的DCPA,这说明在研究开始时DCPD中即存在DCPA杂质,因此DCPA杂质不能归因于本研究的实验期间DCPD向DCPA转化。DCPA片剂的晶体结构不随放置条件和时间变化。
结论
>>>本研究发现不同稀释剂会对ASA的稳定性和片剂质量造成影响。
>>>无水磷酸氢钙A60是能与水份敏感API联合使用的推荐辅料。由于该物料不含任何结晶水,并且由于比表面积降低至0.25 ㎡/g时的水蒸气吸收率非常低,因此将ASA的水解降至最低。即使在95% r.H.高湿度条件下,无水磷酸氢钙A60从环境中最多只吸收0.13%的水蒸气。与此相反,使用MCC时,在40% r.H.条件下将吸收4.68%的水蒸气。
>>>按照通过X射线衍射分析对DCPA进行的评价,在放置时间内或高湿度条件下,晶体结构没有变化。由于无水磷酸氢钙 A60的比表面积小,物料具有脆性特点,提高压压片力将为含无水磷酸氢钙 A60的片剂带来良好的片剂性能。
>>>对于MCC和DCPD而言,在40℃和70% r.H.的放置期间,沿水解路线只能发现很小的ASA降解,这个降解是由于周围环境湿度较高,MCC对水的吸附力弱,无法阻止ASA的大幅水解。一般来说,在片剂尺寸增加时MCC的吸水明显增多。
>>>X射线衍射图显示,在含有DCPD的片剂中,只有少量的结晶水损失。但是,在最初的DCPD物料中,也可以检测到同样量的DCPA。但是,DCPD损失结晶水显示出对ASA稳定性的影响与MCC吸水性对ASA稳定性的影响相同。
>>>未发现所测辅料的粉末表面积增大对ASA的稳定性存在影响。
>>>在适度的压片力下,MCC和DCPD处方的片剂性能最佳。但是,MCC的吸水率对片剂的拉伸强度和脆碎度会有重大影响,在药物制剂开发过程中必须考虑这些因素。
参考文献:
[1] Mutschler E.; Geisslinger G.; Kroemer H.K.; Menzal S.; Ruth P.: Mutschler Arzneimittelwirkungen: Pharmakologie Klinische Pharmakologie Toxikologie,10thed,Stuttgart (Germany) (2012).
[2] Fiebich B.L.; Lieb K.; Hüll M.; Aicher B.; van Ryn J.; Pairet M.; Engelhardt G.: Effects of caffeine and paracetamol alone or in combination with acetylsalicylic acid on prostaglandin E(2)synthesis in rat microglial cells (2000), Neuropharmacology, Volume 39, Issue 11, p.2205–2213.
[3] Carstensen J.T.; Attarchi F.: Decomposition of Aspirin in the Solid State in the Presence of Limited Amounts of Moisture III: Effect of Temperature and a possible mechanism (1988), Journal of Pharmaceutical Sciences, Volume 77, Issue 4, p.318–321.
[4] Ahlneck C.; Alderborn G.: Solid-state stability of acetylsalicylic acid in binary-mixtures with microcrystalline and microfine cellulose (1988), Acta Pharm. Suec.,Volume 25, Issue 1, p.41–52.
[5] Narang A.S.;RaoV.M.; Raghavan K.S.: Excipient Compatibility. In Qio Y.,ChenY.,Zhang G.G.(Eds.),Developing Solid Dosage Forms - Pharmaceutical Theory and Practice, p.126,2009, Elsevier Inc. Academic Press publications.
[6] Landìn M.; Pérez-Marcos B.; Casalderrey M.; Martínez-Pacheco R.; G6mez-Amoza J.L.; Souto C; Concheiro A. Rowe R.C.: Chemical stability of acetylsalicylic acid in tablets prepared with different commercial brands of dicalcium phosphate dihydrate (1994), International Journal of Pharmaceutics,Volume 107, p.247–249.

Copyright © 2025 深圳市优普惠药品股份有限公司 版权所有 互联网药品信息服务资格证书:(粤)-非经营性-2023-0304